Bernadete M.V. Amin
1 – “feedback” por ações hormonais diversas
A regulação das funções corporais pelos hormônios é feita pela regulação das atividades das células individuais. Os hormônios sinalizam às células para que comecem ou parem de secretar, que se contraiam, se dividam ou se diferenciem. Também podem acelerar ou tornar mais lentos esses processos, ou podem modificar as respostas a outros hormônios. Todas essas ações celulares se somam para produzir as respostas biológicas que observamos ao nível dos tecidos, dos órgãos e do corpo todo. Apesar dos hormônios se distribuírem por todo o sangue e por todo o líquido extracelular, apenas certas células-alvo respondem a um dado hormônio. Algumas células são alvos de mais de um hormônio.
Se uma célula responde ou não a um hormônio depende de ter ou não receptores para aquele hormônio. Entretanto é importante reconhecer que a resposta específica provocada em uma célula é determinada mais pela própria célula que pelo hormônio, e que tipos celulares diferentes podem responder ao mesmo estímulo de maneiras diferentes. Por exemplo, tanto as células musculares lisas vasculares, quanto as células dos ductos coletores dos túbulos renais, são alvos do hormônio da hipófise posterior, a vasopressina. Quando estimuladas pela vasopressina, as arteríolas se contraem, enquanto os ductos coletores aumentam sua permeabilidade à água.
A manutenção da integridade do ambiente interno, ou o enfrentamento bem-sucedido de um desafio externo, tipicamente implicam a interação coordenada de vários sistemas fisiológicos e a integração de múltiplos sinais hormonais. As soluções dos problemas fisiológicos requerem a integração de grande variedade de eventos simultâneos que, em conjunto, podem produzir resultados que são maiores ou menores que a simples soma algébrica das respostas hormonais individuais.
2 – “feedback” por modulação
Nem todos os aspectos do controle hormonal são determinados simplesmente pela quantidade de hormônio secretada, nem mesmo pelo momento em que o hormônio é secretado. A receptividade dos tecidos-alvos à estimulação hormonal não é constante e pode alterar-se sob várias circunstâncias. A receptividade dos tecidos-alvo à estimulação hormonal pode ser expressada em termos de dois aspectos distintos, mas relacionados: a sensibilidade à estimulação e a capacidade de resposta. A sensibilidade descreve a acuidade da capacidade de uma célula reconhecer um sinal e de responder em proporção à intensidade daquele sinal. Podemos definir sensibilidade em termos da concentração do hormônio que provocará cerca de 50% da resposta máxima. A capacidade de resposta, ou a resposta máxima que um tecido é capaz de apresentar depende da quantidade de células componentes ou diferenciadas naquele tecido, bem como do nível de desenvolvimento da maquinaria enzimática naquelas células.Os hormônios regulam tanto a sensibilidade quanto a capacidade dos tecidos-alvos responderem a estes ou a outros hormônios.

3 – “feedback” via receptores
Um mecanismo pelo qual os hormônios determinam a sensibilidade dos tecidos-alvo é a regulação dos receptores do hormônio. Deve ser lembrado que o evento inicial na produção de uma resposta hormonal é a interação do hormônio com seu receptor. Quanto maior a concentração do hormônio, maior a probabilidade de ocorrer interação com seus receptores. Se não existirem receptores do hormônio, no entanto, não pode haver resposta, e quanto mais receptores disponíveis para interagir com uma dada quantidade de hormônio, maior a probabilidade de haver resposta. Em outras palavras, a probabilidade da ocorrência da interação hormônio-receptor está relacionada com a abundância do hormônio e do receptor. Apesar da afinidade do receptor por seu hormônio também poder ser modulada, de modo geral parece ser o número de receptores, em vez de sua afinidade pelo hormônio, que é usualmente modulado.
Alguns hormônios diminuem o número de seus próprios receptores nos tecidos-alvos. Este fenômeno, chamado de “regulação para baixo” (down regulation), foi reconhecido como verdadeiro na endocrinologia moderna, quando se mostrou que a sensibilidade diminuída de algumas células à insulina, nos estados hiperinsulínicos, resultava da diminuição do número de receptores na superfície da célula. No entanto, um fenômeno semelhante foi observado, muitos anos antes, por Cannon e Rosenblueth, que descreveram a “supersensibilidade dos tecidos desnervados”. A descoberta original desse fenômeno por Cannon dizia respeito à hipersensibilidade do coração desnervado à epinefrina e norepinefrina circulantes. A generalização deste fenômeno em ambos os sistemas de controle endócrino e neural é indicada adicionalmente pelo aumento dos receptores da acetilcolina que ocorre após um músculo ser desnervado e da restauração à normalidade após a reinervação. O fenômeno da taquifilaxia, ou perda da capacidade de resposta a um agente farmacológico, após exposição repetida ou constante, pode ser outro exemplo da regulação para baixo dos receptores.
A regulação para baixo pode resultar da inativação dos receptores na superfície da célula, da destruição aumentada dos complexos hormônio-receptor internalizados, ou da síntese diminuída dos receptores. A regulação para baixo não é limitada aos efeitos de um hormônio sobre seu próprio receptor, ou aos receptores de superfície para hormônios hidrossolúveis. Um hormônio pode regular para baixo receptores para outro hormônio. Este parece ser o mecanismo pelo qual T3 diminui a sensibilidade dos tireotrofos da hipófise ao hormônio de liberação da tireotrofina. De modo semelhante, a progesterona pode regular para baixo seu próprio receptores e também o do estrogênio.
A regulação para cima (up reguiation), ou o aumento dos receptores disponíveis, também ocorre e pode ser vista tanto nos receptores de superfície. quanto nos receptores internos dos hormônios lipossolúveis. A prolactina e possivelmente o hormônio do crescimento podem regular para cima seus receptores nas células que respondem. O estrogênio regula para cima tanto seus próprios receptores. quanto os do hormônio luteinizante e do hormônio folículo-estimulante nas células do ovário, durante o ciclo menstrual. Os mecanismos moleculares da regulação para cima não são compreendidos, atualmente, e são o assunto de pesquisas intensas. Parece que a regulação para cima, tal como a produzida pelo estrogênio, é iniciada por alteração da expressão dos genes.
A sensibilidade à estimulação hormonal também pode ser modulada de modo que não envolva os receptores. A modulação pós-receptor pode afetar qualquer uma das etapas da via biológica pela qual são produzidos os efeitos hormonais. Por exemplo, a atividade da fosfodiesterase do monofosfato cíclico de adenosina (AMPc.) aumenta no tecido adiposo na ausência dos hormônios hipofisános. Deve ser lembrado que essa enzima catalisa a degradação do AMPc. E, quando sua atividade está aumentada. menos AMPc pode acumular-se, após a estimulação da adenilil ciclase por um hormônio, como a epinefrina. Portanto, se todas as outras condições forem iguais, seria necessária concentração mais alta de epinefrina para produzir uma dada quantidade de lipólise do que aquela necessária em presença de quantidades normais de hormônios hipofisários e daí a sensibilidade à epinefrina parecer reduzida.
A atividade aumentada da fosfodiesterase é apenas um dentre vá rios fatores que contribuem para a sensibilidade diminuída à epinefrina no tecido adiposo de animais hipo-hipofisários. Esses tecidos também têm um defeito na sua capacidade de responder ao AMPc por causa de deficiências da lipase sensível ao hormônio. Portanto, mesmo quando todos os receptores estão ocupados a resposta máxima que esses tecidos podem produzir fica abaixo do normal.
4 – “feedback” via potencialização
Os hormônios também podem aumentar a capacidade das células ou tecidos-alvo responderem a outros estímulos. Por exemplo, o estradiol aumenta a síntese de prolactina nos lactotropos hipofisários e, portanto, aumenta a secreção de prolactina em resposta aos estímulos fisiológicos. Modo ainda mais óbvio pelo qual um hormônio pode aumentar a capacidade do tecido responder a estímulos fisiológicos é aumentar ou diminuir o número de células nos tecidos-alvo. Por exemplo, o aumento gradativo da secreção do estradiol visto na parte inicial do ciclo menstrual, reflete a atividade de número crescente de células da granulosa, em vez de alteração da secreção da gonadotropina.
5 – “feedback” permissivo
Outro aspecto da modulação hormonal relacionado com os exemplos acima foi chamado de ação permissiva. Um hormônio atua permissivamente quando sua presença é necessária para, ou permite, que ocorra uma resposta biológica, mesmo apesar do hormônio não iniciar a resposta. Efeitos permissivos foram originalmente descritos para os hormônios corticais adrenais, mas parecem ocorrer também para outros hormônios. As ações permissivas não são limitadas às respostas aos hormônios, mas ocorrem em qualquer resposta celular a qualquer sinal.
Apesar de um hormônio poder desencadear uma resposta global celular afetando alguma reação fundamental determinadora da intensidade dessa resposta, mais de um processo pode ser afetado. Os efeitos hormonais exercidos em vários locais, em uma mesma célula, se somam para produzir a resposta global. Consideremos, por exemplo, apenas algumas das maneiras pelas quais a insulina atua sobre a célula adiposa para promover o armazenamento de triglicerídeos:
1. Atua na membrana celular, para aumentar a disponibilidade de substrato para a síntese de lipídios
2. Ativa várias enzimas citosólicas e mitocondriais, críticas para a síntese de ácidos graxos
3. Inibe a degradação dos triglicerídeos já formados
4. Induz a síntese da enzima extracelular lipase lipoproteica, necessária à captação de lipídios da circulação
Qualquer um desses efeitos poderia cumprir o objetivo de aumentar o armazenamento de gordura, mas, coletivamente, estes diferentes efeitos tornam possível uma faixa muito mais ampla de resposta, em tempo mais curto.
O reforço também pode ser observado ao nível de todo o organismo, onde um hormônio pode atuar de maneiras diferentes em tecidos diversos para produzir efeitos complementares. Um bom exemplo disso é a ação dos hormônios glicocorticóides promovendo gliconeogênese. Eles atuam nos tecidos periféricos, para mobilizar substrato, e no fígado, para aumentar a conversão dos precursores a glicose. Tanto a ação extra-hepática quanto a ação hepática, aumentariam a gliconeogênese, mas, em conjunto, essas ações complementares reforçam uma à outra e aumentam a magnitude e a rapidez da resposta global.
6 – “feedback” via redundância
As funções cruciais são governadas por mecanismos à prova de erro. Tal como cada sistema de órgãos contém em si um excesso de capacidade, que lhe confere o potencial de funcionar a níveis além das demandas do dia-a-dia, assim também há excesso de capacidade reguladora, fornecido sob a forma de controles aparentemente duplicados ou super-postos. Falando simplesmente, o corpo tem mais de uma maneira de atingir um determinado objetivo. Por exemplo a conversão do glicogênio hepático a glicose sanguínea pode ser sinalizada por, pelo menos, dois hormônios, o glucagon das células alfa do pâncreas e a epinefrina da medula adrenal. Ambos esses hormônios aumentam a produção de AMPc no fígado e desse modo, ativam a enzima fosforilase, que catalisa a glicogenólise. Dois hormônios secretados, a partir de dois tecidos diferentes, às vezes em resposta a diferentes condições, produzem assim o mesmo resultado final.
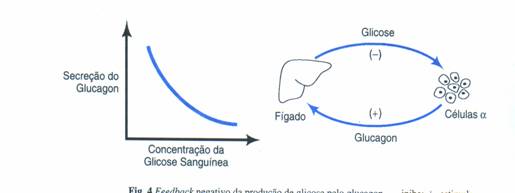
A redundância também pode ser vista a nível molecular. Usando o mesmo exemplo da conversão do glicogênio hepático a glicose sanguínea, há, até mesmo, duas maneiras pelas quais a epinefrina pode ativar a fosforilase. Estimulando os receptores beta-adrenérgicos, a epinefrina aumenta a formação de AMPc como já mencionado. Estimulando os receptores alfa adrenérgicos, a epinefrina também ativa a fosforilase, mas esses receptores operam por meio das concentrações aumentadas de cálcio intracelular produzidas pela liberação de inositol trifosfato.
Os mecanismos redundantes não apenas asseguram que um processo crítico irá ocorrer, mas também oferecem a possibilidade da flexibilidade e do ajuste fino e sutil do processo. Apesar de redundantes, quanto a dois diferentes hormônios poderem ter alguns efeitos superpostos, a ações dos dois hormônios usualmente não são idênticas em todos o aspectos. Dentro da faixa fisiológica de suas concentrações no sangue as ações do glucagon são restritas ao fígado; a epinefrina produz várias outras respostas em muitos tecidos extra-hepáticos, enquanto aumenta glicogenólise no fígado. As variações da entrada relativa de ambos o hormônios permitem um amplo espectro de alterações das concentrações da glicose sanguínea, em relação a outros efeitos da epinefrina, como o aumento da freqüência cardíaca.
Dois hormônios que produzem efeitos comuns podem diferir não apenas na sua gama de ações, mas também quanto a suas constantes de tempo. Um deles pode ter instalação mais rápida e duração mais curta de sua ação, enquanto o outro pode ter duração mais longa da ação, mas instalação mais lenta. Por exemplo, a epinefrina aumenta as concentrações sanguíneas dos ácidos graxos livres (AGL) dentro de segundos a minutos, e esse efeito se dissipa de modo igualmente rápido, quando cessa a secreção de epinefrina. O hormônio do crescimento também aumenta as concentrações sanguíneas dos AGL mas, seus efeitos são vistos apenas após período de latência de 2 ou 3 horas e persistem por muitas horas. Um hormônio como a epinefrina pode, portanto, ser usado para atender as necessidades a curto prazo, e outro, como o hormônio do crescimento, pode responder as necessidades prolongadas.
Uma das implicações da redundância, para a compreensão tanto da fisiologia normal quanto das doenças endócrinas, é que a insuficiência parcial, ou talvez mesmo completa, de um mecanismo pode ser compensada pelo suporte aumentado de outro mecanismo. Assim, as deficiências funcionais podem ser evidentes apenas de modo sutil e podem não se apresentar abertamente como uma doença. Algumas deficiências podem tornar-se aparentes apenas após a provocação apropriada ou a perturbação do sistema. Inversamente, estratégias para intervenções terapêuticas, projetadas para aumentar ou diminuir a intensidade ou a velocidade de um processo, têm que levar em consideração as entradas redundantes que regulam esse processo, A mera aceleração, ou o bloqueio de uma entrada reguladora, pode não produzir o efeito desejado porque ajustes independentes podem compensar completamente a intervenção.
7 – “feedback” via Mecanismos Empurra-Puxa (Push: Pull)
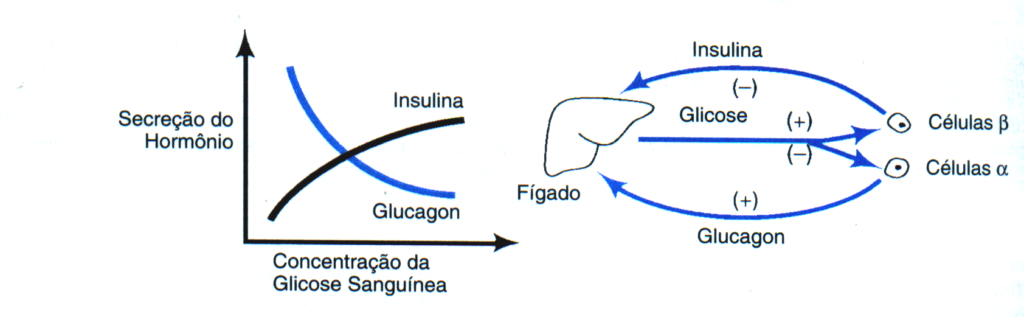
Muitos processos críticos estão sob controle duplo por agentes que atuam antagonisticamente, quer para estimular, quer para inibir. Este controle duplo permite a regulação mais precisa, através do “feedback” negativo. O exemplo citado anteriormente era a produção hepática de glicose, que é aumentada pelo glucagon e inibida pela insulina. Em situações de emergência, ou durante o exercício, a epinefrina e noraepinefrina, liberadas a partir da medula adrenal e das terminações nervosas simpáticas, sobrepujam ambos os sistemas de “feedback” negativo, inibindo a secreção de insulina e estimulando a secreção de glucagon (11). O efeito de acrescentar uma influência estimuladora e remover, simultaneamente, uma influencia inibitória é a obtenção da resposta rápida e intensa, mais rapida e maior do que poderia ser realizado afetando simplesmente cada um dos hormônios isoladamente, ou a da que poderia ser realizada pelo efeito glicogenolítico direto da epinefrina ou da norepinefrina.
Outro tipo de mecanismo empurra-puxa (push: pull) pode ser visto a nível molecular. A síntese final do glicogênio, a partir da glicose, depende da atividade de duas enzimas, a glicogênio sintetase que catalisa a formação de glicogênio a partir da glicose, e a glicogênio fosfarilase, que catalisa a degradação do glicogênio- (Fig. l2). A velocidade final da reação é determinada pelo balanço da atividade das duas enzimas. A atividade de ambas as enzimas está sujeita à regulação pela fosforilação, mas em direções opostas: a adição de um grupamento fosfato ativa a fosforilase, mas inativa a sintetase. Nesse caso, um único agente, o AMPc, que ativa a proteína cinase A, aumenta a atividade da fosforilase e inibe simultaneamente a sintetase.
Referência Bibliográfica
JOHNSON Leonard R. Fundamentos de Fisiologia Médica. 2 ed.Guanabara Koogan; Rio de Janeiro. 1998.